Laboratorio Bradfute

Malattie infettive/patogeni come quelli che sono apparsi di recente in una popolazione o sono esistiti ma stanno aumentando rapidamente per incidenza o per area geografica

Il topo cervo Peromyscus maniculatus è portatore dell'hantavirus Sin Nombre, responsabile della maggior parte dei casi di sindrome cardiopolmonare da hantavirus negli Stati Uniti.
Credito fotografico: Sam Goodfellow

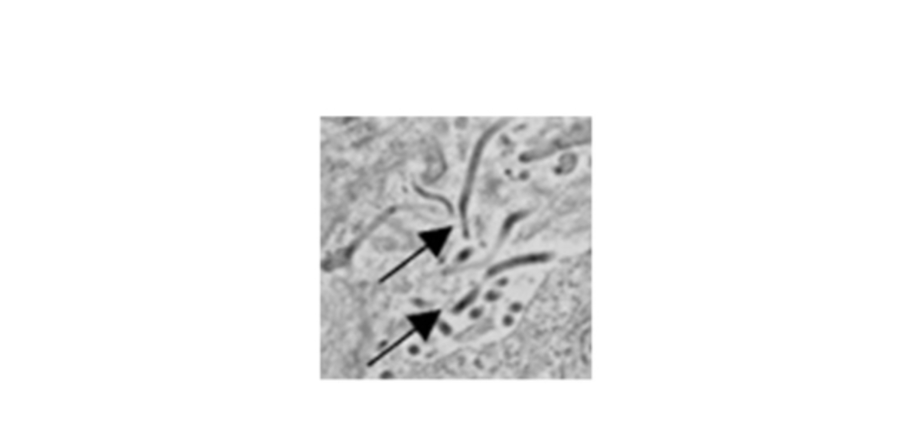
Virus Ebola nella milza infetta. Le frecce indicano i singoli virioni. Imaging eseguito mediante microscopia elettronica a trasmissione.
Credito fotografico: Steven Bradfute, PhD

Test della placca del virus Zika per identificare gli anticorpi neutralizzanti
Credito fotografico: Steven Bradfute, PhD
L'infezione da virus Ebola provoca la morte delle cellule immunitarie. La microscopia a fluorescenza mostra le cellule della milza di un animale infetto. Il rosso segna le cellule morenti e mostra tutte le cellule.
Credito fotografico: Steven Bradfute, PhD
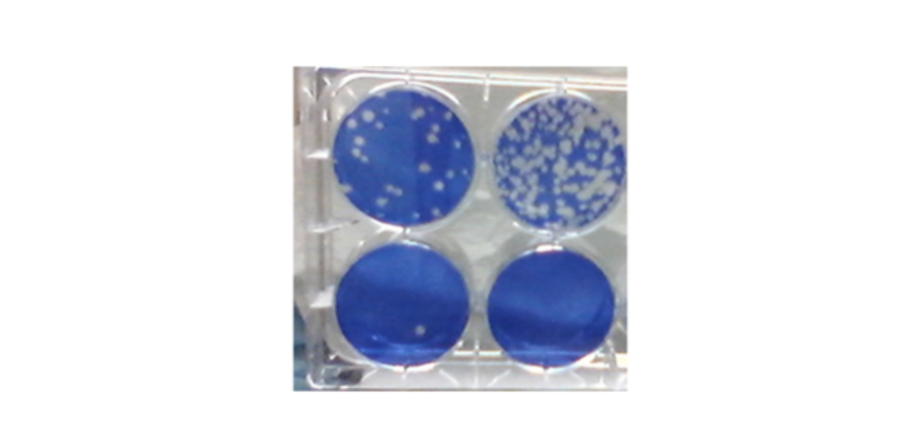
Saggio della placca SARS-CoV-2 per misurare l'inibizione della replicazione del coronavirus. Il colore blu è cellule vive; mentre i buchi sono "le placche mostrano dove SARS-CoV-2 ha infettato e ucciso le cellule.
Credito fotografico: Steven Bradfute, PhD
Gli hantavirus sono agenti patogeni pericolosi che causano gravi malattie negli esseri umani. I virus si replicano in modo innocuo nei roditori e vengono trasmessi all'uomo tramite l'inalazione del virus negli escrementi di roditori aerosolizzati. Il primo hantavirus patogeno negli Stati Uniti, Sin Nombre hantavirus, è stato scoperto nel New Mexico nel 1993. Il New Mexico ha avuto il maggior numero di casi di Sin Nombre hantavirus rispetto a qualsiasi altro stato, rendendolo un virus importante per la nostra regione, soprattutto data la sua elevata letalità tasso negli esseri umani (~35%). La nostra ricerca copre molteplici aree della biologia e della terapia dell'hantavirus.
-Anticorpi neutralizzanti per terapie.
Abbiamo uno sforzo collaborativo come parte di una sovvenzione NIH U19 basata sull'Albert Einstein College of Medicine per identificare e analizzare gli anticorpi monoclonali contro più hantavirus. Questi dati vengono utilizzati dal consorzio per selezionare gli anticorpi per testare la loro capacità di salvare dall'infezione modelli animali di piccole dimensioni. Questo studio collaborativo è evidenziato nel podcast "This Week in Virology": https://www.microbe.tv/twiv/twiv-578/
--Risposte immunitarie della memoria a lungo termine nei sopravvissuti all'hantavirus Sin Nombre.
Stiamo monitorando le risposte immunitarie a lungo termine nei sopravvissuti all'hantavirus Sin Nombre. Ad oggi, abbiamo trovato risposte anticorpali molto forti nei sopravvissuti, con pazienti fino a 23 post-infezione che mostrano ancora risposte anticorpali neutralizzanti rilevabili. Questi dati suggeriscono che i sopravvissuti all'hantavirus generano un'immunità forte e duratura contro la reinfezione. Abbiamo anche stabilito un test citometrico a flusso a 13 colori per testare specifiche risposte di richiamo di hantavirus in più compartimenti di cellule T CD8+ e CD4+ di memoria.
--Analisi genetica del virus Sin Nombre nei roditori catturati in natura nel New Mexico.
Il roditore ospite di Sin Nombre hantavirus è il topo cervo Peromyscus maniculatus. I topi cervi hanno una gamma naturale molto ampia, poiché si trovano in quasi tutti gli Stati Uniti (escluse le regioni del sud-est). Tuttavia, l'infezione da virus Sin Nombre negli esseri umani è principalmente concentrata negli Stati Uniti occidentali e sud-occidentali. Ci stiamo ponendo la domanda "perché i topi cervi sono ovunque ma gli umani infetti no?" Rispondiamo a questa domanda intrappolando topi cervi selvatici in tutto il New Mexico, nelle regioni endemiche e non endemiche dell'infezione umana, per determinare se a) il virus Sin Nombre si trova solo nelle regioni endemiche dei pazienti umani o b) la sequenza del genoma del virus è significativamente diverso nelle diverse regioni.

Il laboratorio Bradfute ha sfruttato la nostra esperienza nei patogeni virali emergenti per studiare il virus Zika durante l'epidemia 2013-2016. Abbiamo collaborato con i laboratori nazionali di Los Alamos per testare l'efficacia di un nuovo sistema di rilascio di DNA/nanoparticelle nella protezione dei topi dall'infezione da virus Zika. Abbiamo scoperto che un vaccino a DNA plasmidico formulato in un nuovo sistema di somministrazione induce un'immunità protettiva contro l'infezione da virus Zika nei topi in modo dose-dipendente.
Hraber P, Bradfute SB, Clarke E, Ye C e Pitard B. Copolimero a blocchi anfifilico Consegna di un vaccino a DNA contro il virus Zika. Vaccino 36:6911 (2018)

Il laboratorio Bradfute è coinvolto nella sperimentazione di nuovi vaccini per l'induzione di risposte immunitarie cross-reattive contro più virus dell'encefalite, che sono trasmessi dalle zanzare e causano gravi malattie sia nei cavalli che nell'uomo.
-- Consegna dell'antigene nanocarrier per vaccini alfavirus a dose singola ampiamente protettivi.
Stiamo collaborando con i Los Alamos National Laboratories (LANL) per testare un nuovo vaccino a base di DNA per fornire un'immunità a iniezione singola e di lunga durata contro più alfavirus. Il nostro ruolo in questa collaborazione è quello di testare i vaccini a DNA per la loro induzione di anticorpi e risposte delle cellule T nei topi, utilizzando gli alfavirus BSL-3 come bersagli.
-- RNA lunghi non codificanti nell'infezione da virus dell'encefalite equina venezuelana.
Abbiamo appena ricevuto una sovvenzione per un ampio progetto che studia il ruolo degli RNA lunghi non codificanti nelle risposte cellulari all'infezione da virus dell'encefalite equina venezuelana. Questo progetto sfrutterà le nostre strutture selezionate dell'agente BSL-3 presso UNM HSC per testare quali RNA lunghi non codificanti sono espressi dopo l'infezione in vitro e in vivo di un virus patogeno dell'encefalite equina venezuelana rispetto a una versione non patogena dello stesso virus. In questo modo, saremo in grado di confrontare direttamente quali RNA lunghi non codificanti sono indotti o soppressi in una risposta cellulare di successo rispetto a una risposta non riuscita.
Il virus Ebola è un patogeno mortale che ha un tasso di mortalità superiore al 40%. Sebbene tradizionalmente limitato a piccoli focolai in villaggi isolati, il virus ha iniziato a diffondersi per la prima volta nelle grandi città, causando un'epidemia globale dal 2013 al 2016. Siamo coinvolti negli sforzi per lo sviluppo di vaccini e terapie per questo virus.
-Vaccino contro il virus Ebola e sviluppo di terapie.
Abbiamo scoperto che i cambiamenti della glicosilazione (modello dello zucchero) nella glicoproteina virale influenzano notevolmente il modo in cui queste proteine inducono una risposta immunitaria quando vengono utilizzate come vaccino. Questi cambiamenti nella glicosilazione si verificano quando i vaccini vengono prodotti in diversi tipi di cellule. I nostri risultati sono stati rilevanti, poiché diversi tipi di cellule vengono utilizzati per diversi vaccini.
-Co-somministrazione terapeutica e vaccinale del virus Ebola.
I nostri studi sul virus Ebola sono proseguiti con il recente finanziamento di una seconda sovvenzione, in cui stiamo studiando come la somministrazione di terapie a breve termine insieme a vaccini a lungo termine influenzi l'efficacia di questi trattamenti. L'obiettivo è determinare la tempistica ottimale per la somministrazione di entrambi i farmaci terapeutici per la protezione immediata contro il virus senza annullare la protezione a lungo termine dei vaccini co-somministrati

Data l'urgenza della pandemia di coronavirus in corso, il laboratorio Bradfute ha guidato il lavoro sul virus BSL-3 SARS-CoV-2 presso l'UNM HSC. Abbiamo collaborato con oltre 25 diversi gruppi accademici e commerciali per utilizzare la nostra specializzazione unica per ricercare terapie, vaccini, inattivazione, biologia di base e analisi di campioni di pazienti per SARS-CoV-2.
-- Valutazione degli anticorpi neutralizzanti in pazienti convalescenti e acuti COVID-19.
Il laboratorio Bradfute ha testato i titoli anticorpali neutralizzanti nel plasma di individui convalescenti e nel plasma di pazienti acuti COVID-19 che erano stati infusi con il plasma convalescente come terapia sperimentale presso l'UNMH. Abbiamo scoperto che sebbene tutti i pazienti convalescenti testati avessero titoli anticorpali positivi contro la proteina di superficie Spike quando misurati mediante saggi di immunoassorbimento enzimatico (ELISA), i livelli di anticorpi neutralizzanti contro SARS-CoV-2 vivo erano molto bassi negli individui convalescenti e quindi non aumentare i livelli di anticorpi o migliorare la progressione della malattia nei riceventi. Questo studio ha evidenziato l'importanza del plasma convalescente pre-screening non solo per l'anticorpo totale tramite ELISA, ma per neutralizzare i titoli anticorpali prima dell'infusione nei pazienti. Abbiamo anche collaborato con i laboratori di riferimento TriCore per dimostrare che i titoli anticorpali neutralizzanti sono correlati a un test di rilevamento anticorpale semplice e rapido utilizzato in commercio che non richiede l'uso di virus vivi.
-- Metodi per l'inattivazione di SARS-CoV-2 sulle superfici.
Abbiamo testato diversi metodi chimici, termici, luminosi e di altro tipo per inattivare il SARS-CoV-2 vivo. Abbiamo anche dimostrato che un metodo comunemente suggerito per decontaminare le maschere N95 con calore secco non è efficace nell'eliminare il SARS-CoV-2 vivo.
-- Analisi delle risposte longitudinali di anticorpi e cellule T in individui convalescenti COVID-19. Siamo stati recentemente finanziati dall'UNM HSC CTSC per monitorare le risposte immunitarie nei pazienti dopo il loro recupero dall'infezione da SARS-CoV-2. Abbiamo un IRB approvato per questo lavoro e stiamo attualmente reclutando 50 pazienti per analizzare le loro risposte anticorpali e delle cellule T per un massimo di 10 anni. Questo lavoro risponderà a domande vitali su quanto tempo i sopravvissuti al COVID-19 hanno risposte immunitarie contro il virus.
-- Screening in vitro di piccole molecole contro SARS-CoV-2.
Uno degli aspetti principali del mio lavoro su SARS-CoV-2 è incentrato sul test di piccole molecole per la loro efficacia in vitro contro virus vivi nel laboratorio BSL-3. Abbiamo lavorato con UNM HSC, campus principale UNM e istituzioni non UNM per testare i loro farmaci per l'attività antivirale. Il mio laboratorio ha esaminato molte piccole molecole e ne ha trovate una manciata che inibiscono potentemente la replicazione. Questo lavoro ha portato a molte richieste di sovvenzioni e manoscritti in preparazione o presentati, un esempio dei quali è elencato di seguito.